Radioatividade: Fenômeno Nuclear
Como a radioatividade foi descoberta
No ano de 1896, o francês Henri Becquerel constatou que um composto de urânio — sulfato de potássio e uranilo, K2UO2(SO4)2 — apresentava a interessante característica de causar uma mancha numa chapa fotográfica mesmo no escuro e embrulhada em papel negro.
A interpretação de Becquerel era de que o composto emitia algum tipo de raio capaz de atravessar o papel e atuar sobre a chapa. Essa propriedade era semelhante à dos raios X descobertos um ano antes por Wilhelm Conrad Röntgen.
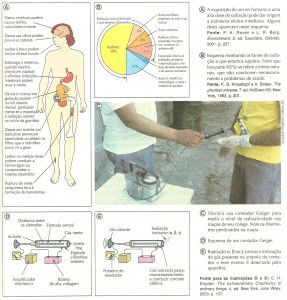
Ainda no mesmo ano, Becquerel percebeu que os raios do urânio ionizavam gases, isto é, provocavam neles o aparecimento de íons, tornando-os condutores de corrente elétrica. Anos mais tarde, o alemão Hans Geiger utilizaria essa propriedade para criar o famoso contador Geiger.
 No final de 1897, a polonesa Marie Sklodowska Curie passou a se interessar pelo fenômeno descoberto por Becquerel. Em abril de 1898, ela já havia percebido que, além do urânio, outro elemento conhecido, o tório, também emitia os misteriosos raios. Começou, então, a suspeitar da existência de elementos radioativos desconhecidos. Em julho do mesmo ano, com a ajuda do marido, físico francês de renome chamado Pierre Curie, descobriu um novo elemento que chamou de polônio. Alguns meses depois, ambos descobriram um elemento ainda mais radioativo ao qual deram o nome de rádio.
No final de 1897, a polonesa Marie Sklodowska Curie passou a se interessar pelo fenômeno descoberto por Becquerel. Em abril de 1898, ela já havia percebido que, além do urânio, outro elemento conhecido, o tório, também emitia os misteriosos raios. Começou, então, a suspeitar da existência de elementos radioativos desconhecidos. Em julho do mesmo ano, com a ajuda do marido, físico francês de renome chamado Pierre Curie, descobriu um novo elemento que chamou de polônio. Alguns meses depois, ambos descobriram um elemento ainda mais radioativo ao qual deram o nome de rádio.
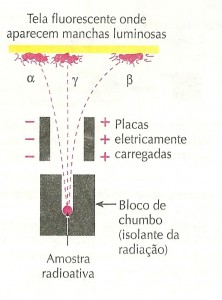
Ainda no ano de 1898, Ernest Rutherford utilizou uma tela fluorescente para detectar as radiações provenientes de um material radioativo. Com auxílio de placas metálicas eletricamente carregadas descobriu que havia dois tipos de radiação, que chamou de alfa (α) e beta (β). A radiação α, segundo ele, deveria ser formada por partículas de carga positiva, uma vez que seu feixe é atraído pela placa negativa (veja o esquema ao lado). Já a radiação β deveria ser formada por partículas negativas, pois seu feixe é atraído pela placa positiva. Além disso, como as partículas α sofrem um desvio menor, isso significa que elas devem possuir massa maior do que as partículas β, pois, quanto maior for a massa de uma partícula, maior será a sua inércia e, portanto, mais difícil será alterar sua trajetória.
Em 1900, Paul Villard, na França, descobriu uma outra forma de radioatividade que não apresenta carga elétrica, chamada de radiação gama (γ). Nesse mesmo ano, Becquerel descobriu que as partículas β são, na verdade, elétrons com alta velocidade. Em 1909, Rutherford mostrou que as partículas α são íons de hélio bipositivos.
Radioatividade e estrutura atômica
Número atômico (Z) é um número que indica quantos prótons há no núcleo de um átomo e número de massa (A) corresponde à soma dos números de prótons e nêutrons. Átomos que possuem mesmo número atômico pertencem ao mesmo elemento químico.
Radioatividade é um fenômeno nuclear. As reações nucleares são processos em que o núcleo de um átomo sofre alteração.
Nuclídeo é o nome dado a um núcleo caracterizado por um número atômico (Z) e um número de massa (A).
Radionuclídeo ou radioisótopo é um nuclídeo emissor de radiação.
Perceba a diferença entre uma reação química e uma reação nuclear. As reações químicas estão relacionadas à eletrosfera. Antes e depois delas, os átomos estão unidos de maneira diferente, e essa união envolve os elétrons. Já uma reação nuclear provoca alterações no núcleo do átomo, como veremos neste capítulo.
Isótopos são átomos com um mesmo número atômico e diferentes números de massa. A palavra isótopo, além desse significado, pode também ser usada como sinônimo da palavra nuclídeo.
Estudo Das Emissões Alfa, Beta e Gama
As radiações α e β
 Atualmente sabe-se que há núcleos instáveis. A emissão de partículas α ou β é o modo encontrado pelo núcleo para aliviar essa instabilidade.
Atualmente sabe-se que há núcleos instáveis. A emissão de partículas α ou β é o modo encontrado pelo núcleo para aliviar essa instabilidade.
As partículas alfa são constituídas por 2 prótons e 2 nêutrons, isto é, o núcleo de um átomo de hélio ![]() . São simbolizadas por
. São simbolizadas por ![]() . Quando um núcleo as emite, perde 2 prótons e 2 nêutrons.
. Quando um núcleo as emite, perde 2 prótons e 2 nêutrons.
Sobre as emissões a, foi enunciada por Soddy, em 1911, a chamada Primeira Lei da Radioatividade: “Quando um radionuclídeo emite uma partícula a, seu número de massa diminui 4 unidades e seu número atômico diminui 2 unidades.” A figura A, ao lado, ajuda a entender por que a emissão alfa provoca essas variações no núcleo.
As partículas β são elétrons emitidos pelo núcleo de um átomo instável, sendo representadas por ![]() . Você deve estar se perguntando: Como pode o núcleo de um átomo emitir um elétron? A resposta reside no fato de que, em núcleos instáveis beta-emissores, um nêutron pode se decompor em um próton, um elétron e um antineutrino. O próton permanece no núcleo, o elétron (partícula β) e o antineutrino são emitidos. O antineutrino é uma partícula com número de massa zero e carga nula. Não vamos nos preocupar com o antineutrino, pois, assim como ele, atualmente se conhecem muitas outras partículas subatômicas além dos prótons, nêutrons e elétrons, e o estudo dessas outras partículas é complexo e está além dos objetivos.
. Você deve estar se perguntando: Como pode o núcleo de um átomo emitir um elétron? A resposta reside no fato de que, em núcleos instáveis beta-emissores, um nêutron pode se decompor em um próton, um elétron e um antineutrino. O próton permanece no núcleo, o elétron (partícula β) e o antineutrino são emitidos. O antineutrino é uma partícula com número de massa zero e carga nula. Não vamos nos preocupar com o antineutrino, pois, assim como ele, atualmente se conhecem muitas outras partículas subatômicas além dos prótons, nêutrons e elétrons, e o estudo dessas outras partículas é complexo e está além dos objetivos.
Assim, ao emitir uma partícula β, o núcleo tem a diminuição de um nêutron e o aumento de um próton, como aparece esquematizado na figura (B). Desse modo, o número de massa permanece constante.
A Segunda Lei da Radioatividade, enunciada por Soddy, Fajjans e Russel, em 1913, diz: “Quando um radionuclídeo emite uma partícula β, seu número de massa permanece constante e seu número atômico aumenta de 1 unidade”.
A radiação γ
Ao contrário das radiações α e β que são constituídas por partículas, a radiação γ é formada por ondas eletromagnéticas emitidas por núcleos instáveis logo em seguida à emissão de uma partícula α e β.
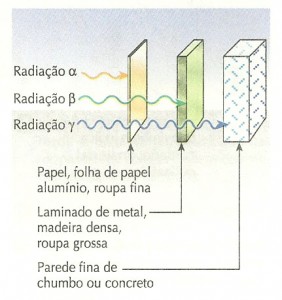
As radiações α, β e γ possuem diferente poder de penetração. Uma partícula α pode penetrar até 0,05 cm na pele e uma β, até 1,5 cm. A radiação γ, por sua vez, facilmente atravessa todo o nosso organismo.
Tomemos como exemplo o césio-137, o beta-emissor envolvido no acidente de Goiânia. Ao emitir uma partícula β, seus núcleos se transformam em bário-137. No entanto, pode acontecer de, mesmo com a emissão, o núcleo resultante não eliminar toda a energia de que precisaria para se estabilizar. A emissão de uma onda eletromagnética (radiação γ) ajuda um núcleo instável a se estabilizar.
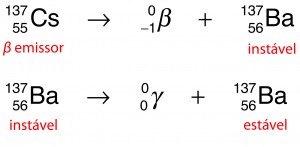
É importante dizer que, das várias ondas eletromagnéticas (radiação γ, raios X, microondas, luz visível etc), apenas os raios γ são emitidos pelos núcleos atômicos. Quando um átomo emite α, β ou γ, dizemos que ele sofreu decaimento radioativo. Como mostra o esquema ao lado, as radiações α, β e γ possuem diferentes capacidades para atravessar os materiais.
Efeitos biológicos da radiação ionizante
As partículas α e β e os raios γ possuem a propriedade de ionizar as moléculas que encontram em seu caminho, isto é, arrancar elétrons delas, originando íons.
Ao atravessar tecidos biológicos, as partículas radioativas provocam a ionização de moléculas existentes nas células. Essa ionização pode conduzir a reações químicas anormais e à destruição da célula ou alteração das suas funções. Isso é particularmente preocupante no caso de lesões no material genético, o que pode causar uma reprodução celular descontrolada, provocando o câncer.
Alterações do material genético das células reprodutivas (espermatozóide e óvulo) podem causar doenças hereditárias nos filhos que o indivíduo possa vir a gerar. Os raios γ são geralmente os mais perigosos, em virtude de seu elevado poder de penetração.
Detecção da radiação
O mais conhecido dos instrumentos detectores de radiação é o contador Geiger (ou Geiger-Müller).
Seu funcionamento é baseado na capacidade que as radiações têm de ionizar gases. Quando a radiação (alfa, beta ou gama) ioniza o gás que existe dentro de uma ampola especial, esse gás se torna, momentaneamente, condutor de corrente elétrica. Isso é detectado pelo aparelho e convertido em um sinal sonoro e em uma medida que aparece num mostrador. Quanto mais radiação atingir o gás da ampola, maior será a condutividade elétrica do gás, o nível de ruído ouvido e o nível de radiação indicado pelo mostrador.
Para pessoas que trabalham em locais sujeitos à radiação há outros métodos de medida da radiação recebida. Entre eles podemos citar os dosímetros (que se parecem com crachás ou bastonetes). Eles são pendurados na roupa e contêm substâncias especiais que mudam de cor à medida que recebem radiação. Assim, eles informam se a pessoa recebeu radiação, e também dão uma noção aproximada da dose recebida.
Texto de: Peruzzo, F. M., & Canto, E. L. (2003). Radioatividade: fenômeno de origem nuclear. In: F. M. Peruzzo, & E. L. Canto, QUÍMICA na Abrodagem do Cotidiano (3ª ed., Vol. 2, p. 344). São Paulo: Moderna.