Isomeria Cis-Trans
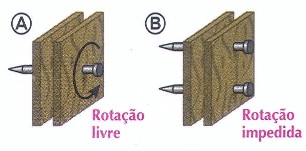 Imagine duas tábuas pelas quais atravessamos um prego (figura A). Existe a possibilidade de girá-las livremente ao redor desse prego. Agora imagine que atravessemos dois pregos (B). Nesse caso, o movimento giratório está travado. O mesmo acontece com as ligações covalentes entre carbonos. Ao longo de uma ligação simples (C) existe liberdade rotacional, mas ao longo de uma dupla (D), não.
Imagine duas tábuas pelas quais atravessamos um prego (figura A). Existe a possibilidade de girá-las livremente ao redor desse prego. Agora imagine que atravessemos dois pregos (B). Nesse caso, o movimento giratório está travado. O mesmo acontece com as ligações covalentes entre carbonos. Ao longo de uma ligação simples (C) existe liberdade rotacional, mas ao longo de uma dupla (D), não.
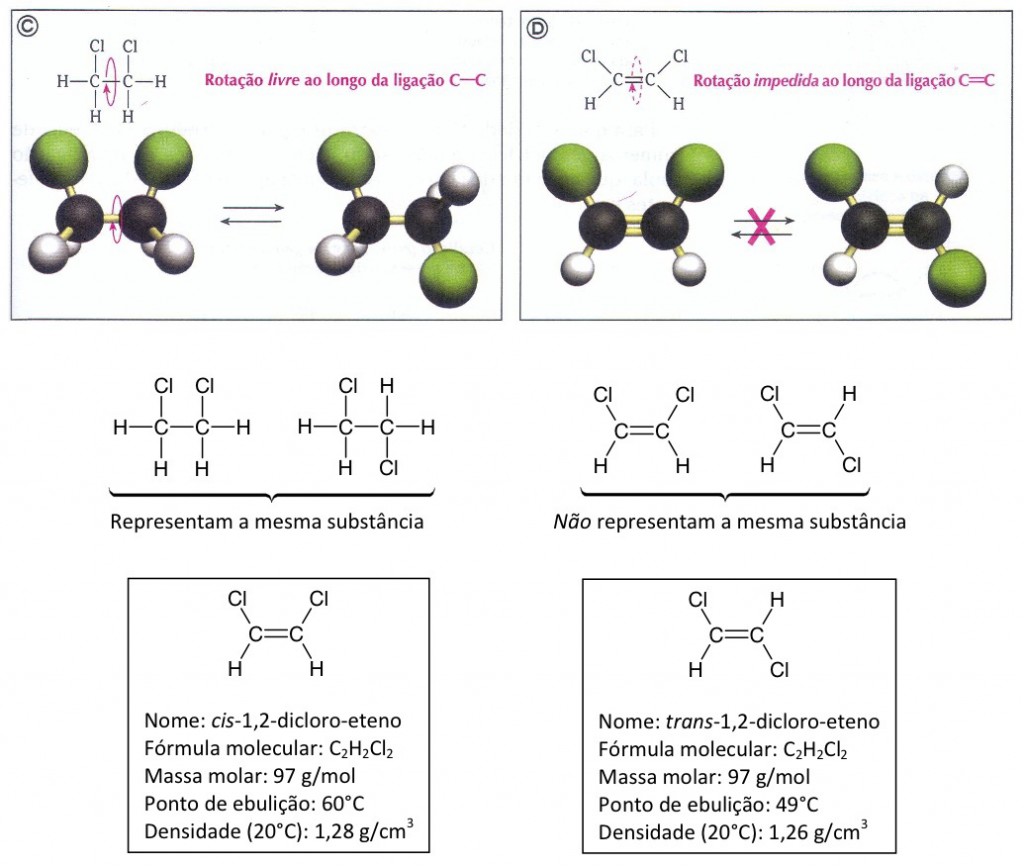
Como você pode perceber, a diferença entre esses dois compostos está na disposição geométrica dos grupos ligados aos carbonos da dupla. A isso chamamos de isomeria geométrica, e esses isômeros são diferenciados por meio dos prefixos cis e trans.
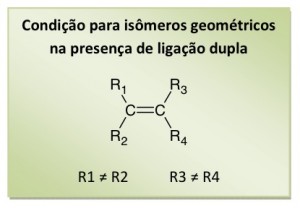
Toda vez que essa condição é satisfeita, trocando de posição os ligantes de um dos carbonos ao escrever a estrutura, chega-se a outro composto, seu isômero geométrico. Para ficar mais claro, veja os seguintes exemplos de casos em que não há isomeria geométrica:
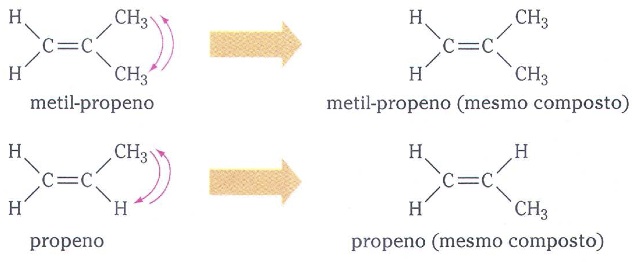
Observe, agora, exemplos de casos em que há isomeria geométrica:
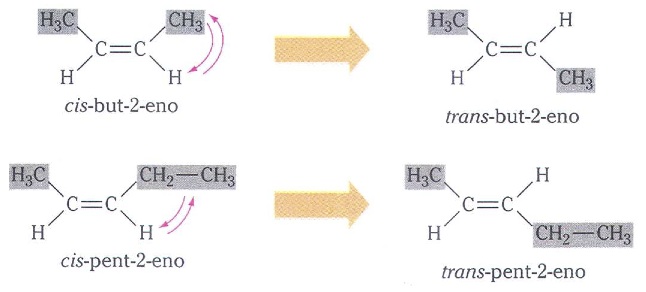
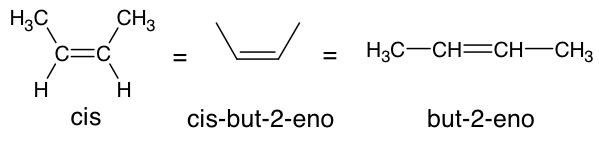
Examinando os exemplos acima você também pode perceber como é feita a nomenclatura. Chamamos de cis o composto em que os maiores grupos de cada carbono estão posicionados de um mesmo lado de uma linha imaginária que passa pela ligação dupla C=C, e de trans o composto em que os maiores grupos de cada carbono estão em lados opostos dessa linha.
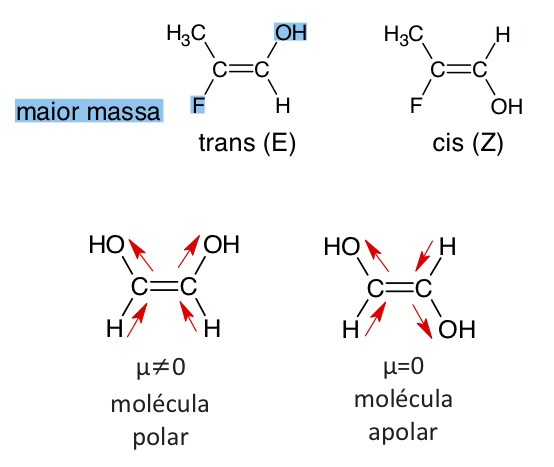
Atenção!
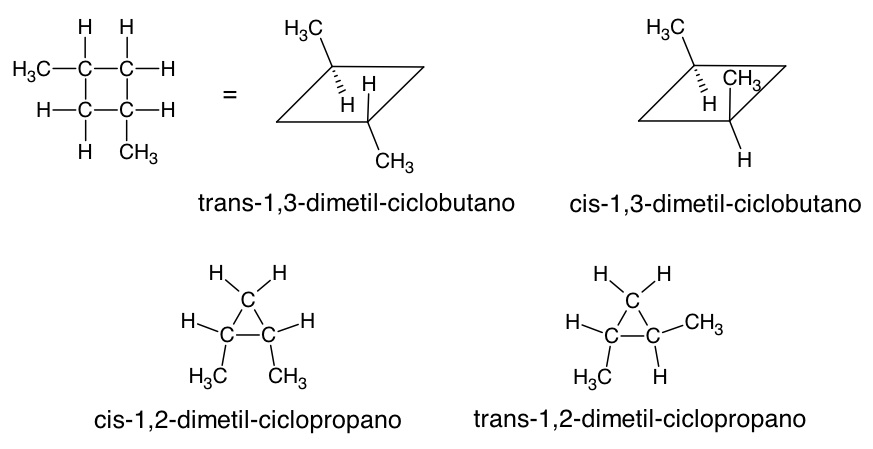
Isomeria geométrica em compostos cíclicos
Basta verificar se no ciclo há dois carbonos (não necessariamente vizinhos) com dois ligantes diferentes.
Atenção!
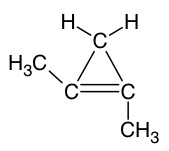
O composto não apresenta isomeria geométrica, pois os carbonos da dupla ligaçãopossuem apenas um ligante fora do ciclo.



